
武漢嘉德人和科技有限公司
武漢嘉德人和科技有限公司報道(dào):規模巨大的中國(guó)市場打開(kāi),跨國(guó)藥企各巨頭都(dōu)在布陣。中國(guó)的創新藥市場已經(jīng)成(chéng)爲企業的兵家必争之地。
優先審評審批和進(jìn)口藥注冊提速帶來的新藥在華紮堆上市,在2017年達到了第一個小高潮。
2017年全年,在中國(guó)首次注冊的進(jìn)口創新藥達到了39個,包括34個化藥和5個生物藥,多數都(dōu)是通過(guò)優先審評流程獲批,速度最快的從CDE受理到獲批僅用了5個月。

并且,截至2018年1月底,還(hái)有20個進(jìn)口創新藥在審評審批隊列,其中大多數已經(jīng)被(bèi)納入優先審評審批。有望在2018~2019年獲批。
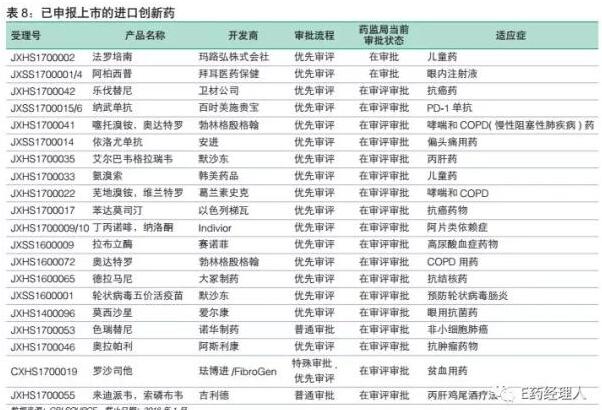
從适應症上看,這(zhè)些産品的治療領域遍布腫瘤、高血壓、糖尿病、自身免疫性疾病、丙肝、肺動脈高壓等熱門治療領域,多個産品是直接競争對(duì)手,多數産品還(hái)是同類型産品中全球首個上市的重磅品種(zhǒng)。這(zhè)不僅大大豐富了患者的治療選擇,還(hái)能(néng)在價格上形成(chéng)競争機制,擴大藥物的可及性。
武漢卡諾斯科技注意到,規模巨大的中國(guó)市場打開(kāi),跨國(guó)藥企各巨頭都(dōu)在布陣。中國(guó)的創新藥市場已經(jīng)成(chéng)爲企業的兵家必争之地。随著(zhe)藥品審評制度改革的進(jìn)一步深化,以及中國(guó)越來越多的參與到國(guó)際多中心臨床研究中,全球新藥的“中國(guó)時(shí)差”越來越短。

武漢嘉德人和科技有限公司按企業産品獲批數量劃分,BI、諾華、強生處于第一梯隊
1、中國(guó)成(chéng)BI最大新興市場
在大量此前卡在審批環節的新藥陸續獲批的情形下,中國(guó)已經(jīng)成(chéng)爲BI最大的新興市場。
2017年,BI共有5款化藥創新藥獲CFDA批準,包括2款降糖藥歐唐靜(恩格列淨)和歐雙甯(利格列汀/二甲雙胍),一款降壓藥雙加(替米沙坦-氨氯地平),兩(liǎng)款治療非小細胞肺癌的抗癌藥尼達尼布(維加特)和阿法替尼(吉泰瑞)。
其中,阿法替尼的上市具有節點性意義,其是首個“上市申請”獲得優先審評的進(jìn)口新藥,同時(shí)也是第一個以“優先審評”資格被(bèi)CFDA批準上市的進(jìn)口新藥。作爲在華首個EGFR-TKI,其療效顯著優于第一代。它的上市,表示海外新藥進(jìn)入中國(guó)的速度將(jiāng)大大加快。
在中國(guó)獲批之前,阿法替尼已經(jīng)被(bèi)70多個國(guó)家批準用于治療EGFR突變陽性非小細胞肺癌,且在很多地區已經(jīng)成(chéng)爲EGFR靶向(xiàng)藥的首選。國(guó)際上首次獲批時(shí)間爲2013年7月在美國(guó)上市,間隔3年8個月後(hòu)在中國(guó)獲批。相比國(guó)際新藥在中國(guó)獲批平均間隔的5年時(shí)間,提前2年。
2016年,新型口服降糖藥SGLT-2抑制劑的全球銷售額爲45.8億美元,但這(zhè)類藥品在中國(guó)剛剛起(qǐ)步。2017年3月獲批的阿斯利康的糖尿病新藥達格列淨,是中國(guó)首個上市的SGLT-2抑制劑。恩格列淨作爲第二款在華上市的SGLT-2抑制劑,其上市晚于達格列淨,目前兩(liǎng)産品是直接競争對(duì)手。在本土企業中,有恒瑞、東陽光藥、軒竹醫藥已經(jīng)在臨床試驗啓動,進(jìn)度最快的是恒瑞的恒格列淨,去年6月啓動III期臨床試驗,爲期52周。
治療特異性肺纖維化(IPF)的乙磺酸尼達尼布軟膠囊在2017年4月17日獲CDE承辦受理,6月6日被(bèi)納入優先審評,9月22日獲批。一共曆時(shí)5個月,可謂神速。
全球IPF市場2025年將(jiāng)達到32億美元,尼達尼布2017年上半年全球銷售額4.29億歐元(人民币33.6億元),是當年表現最好(hǎo)的藥物之一。中國(guó)大約有50萬IPF患者,且發(fā)病人數呈增加趨勢,在尼達尼布獲批之前,國(guó)内治療IPF的産品隻有羅氏的吡非尼酮。目前兩(liǎng)款産品均價格昂貴。值得注意的是,本土企業廣東衆生藥業研制的治療IPF的新藥伊非尼酮已經(jīng)被(bèi)CDE獲批臨床。
無疑,這(zhè)些産品在華獲批,將(jiāng)拉動BI在華業績在未來幾年之内強勢增長(cháng)。而數據顯示,截止到2018年1月,BI還(hái)有兩(liǎng)款創新藥産品奧達特羅和噻托溴铵在審評審批中,且均在優先審評流程。
兩(liǎng)款都(dōu)是COPD(慢性阻塞性肺部疾病)藥物。全球和國(guó)内的COPD市場都(dōu)正在擴容,但一直缺少重磅産品。噻托溴铵一直是BI最暢銷産品,且被(bèi)EvaluatePharma預測爲,在COPD領域唯一有可能(néng)進(jìn)入“2020年50個最暢銷藥物榜單”的藥物。
同時(shí),2018年,BI還(hái)將(jiāng)在華發(fā)力生物藥。
武漢嘉德人和科技有限公司判斷,2017年5月,BI中國(guó)生物制藥基地在上海張江高新技術園區正式啓動,這(zhè)是BI繼德國(guó)、奧地利、美國(guó)之後(hòu)的第四個生物制藥基地,彰顯其以此基地作爲“橋梁”,迅速進(jìn)入中國(guó)生物醫藥市場的決心。2018年開(kāi)年,BI就(jiù)和百濟神州就(jiù)後(hòu)者在研PD-1抗體tislelizumab簽署商業供應協議,tislelizumab在生物制藥生産基地進(jìn)行生産,作爲對(duì)藥品上市許可持有人制度的探索。
在此前,BI已經(jīng)將(jiāng)27種(zhǒng)生物制藥産品推向(xiàng)全球市場,第四個生物制藥基地在中國(guó)的建立也將(jiāng)加速其生物制藥産品在中國(guó)的上市。
建議浏覽器分辨率:1024*768 網絡支持:阿裡(lǐ)巴巴站 Chemicalbook 百度愛采購 LookChem 蓋德化工網 中國(guó)制造網 環球資源網 中國(guó)化工網 慧聰網 華夏化工網
聲明:本站産品資料及信息僅供參考,不能(néng)作爲檢測檢驗的依據,購買請撥打銷售熱線。如有轉載或引用文章涉及版權問題,請與我們聯系。







